Surveillance continue de la glycémie chez les diabétiques de type 2
Un avantage également pour les personnes n’étant pas sous insulinothérapie intensive(1, 2)
Le système FreeStyle Libre* est une forme de surveillance continue de la glycémie (SCG) utilisée dans le traitement des personnes atteintes de diabète de type 1 (DT1) et de type 2 (DT2), principalement en association avec une insulinothérapie intensive.(3) Mais quels sont ses avantages pour l’autre groupe de patients atteints de DT2 ? Nous les passons en revue avec le Pr Christophe De Block, chef du service d'Endocrinologie de l'UZA.
Éducation et compréhension
La surveillance continue de la glycémie (SCG) est indiquée pour la surveillance de la glycémie et est aujourd’hui considérée comme la norme de soins pour les personnes atteintes de DT1. Son utilisation dans le DT2 se généralise également, surtout en cas d’insulinothérapie intensive. Entre-temps, différentes études randomisées démontrent également les avantages de la SCG lorsque seule l’insuline basale est utilisée ou quand le traitement repose sur d’autres médicaments.(1, 2)
« Lorsque les personnes qui reçoivent 3 ou 4 injections d’insuline utilisent la SCG, cela aide bien sûr à déterminer les doses d’insuline appropriées », confirme le professeur De Block, « mais la SCG nous apprend, ainsi qu’au patient, bien plus encore. Elle montre l’évolution de la glycémie sur une période de 24 heures, fournit des informations sur l’effet du traitement, mais indique également l’effet de l’alimentation et de l’activité physique sur la glycémie. Nous voyons les pics postprandiaux, la glycémie avant le coucher, l’évolution tout au long de la nuit… c’est bien plus que ce que montrent les tests par piqûre au doigt. »
Eat to target. Move to target.
« Tous les médecins connaissent le mantra « treat to target ». Eh bien, depuis l’arrivée de la SCG, on parle désormais aussi, dans le cas du diabète de type 2, de « eat to target, move to target », relève le professeur De Block, « C’est très simple : on voit l’effet immédiat de l’alimentation et de l’activité physique, et on peut tester ce qui se passe au niveau de la glycémie si, par exemple, on mange une demi-portion de pâtes au lieu d’une portion entière, ou quel est l’effet d’une demi-heure de marche rapide après le repas. De cette manière, on peut ajuster ces éléments afin que les valeurs glycémiques restent en dessous des seuils convenus au préalable. On voit immédiatement le résultat des actions entreprises, ce qui peut être extrêmement motivant. »(4)
Interprétation rapide des données
Avec le système FreeStyle Libre 2, les données glycémiques sont collectées pendant 14 jours(5) et présentées de manière standardisée et claire. D’un seul coup d’œil, il est possible de déterminer si le contrôle glycémique est satisfaisant ou non. Au niveau international, des objectifs ont été fixés par consensus pour les diabétiques de type 2.(6)
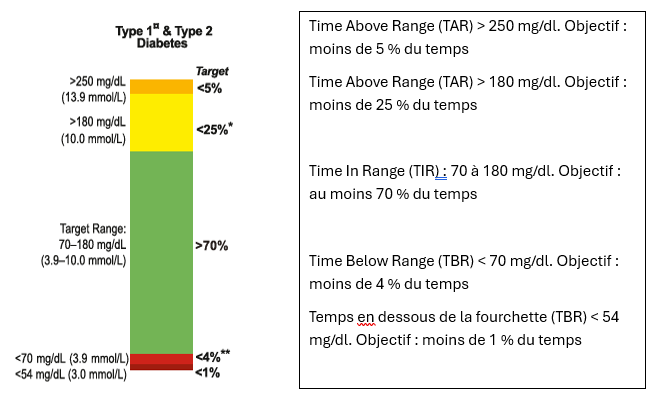
Battelino et al; 2029.
NOOT VOOR LAY-OUT: In de figuur met de kleurbalken mogen de waarden in mmol/L weggelaten worden en moet het woord “Target” vertaald worden door “Objectif”. De kleuren moeten zeker gerespecteerd worden.
De titel (Type 1 & Type 2 Diabetes) moet vervangen worden door "Diabète de type 1¤ et de type 2"
Outre ces objectifs, le rapport glycémique contient de nombreuses autres données, l'Ambulant Glucose Profile (AGP) offrant un aperçu de l'évolution de la glycémie tout au long de la journée, et ce pour la période des 14 derniers jours.
Rôle du médecin généraliste
« Le médecin généraliste joue un rôle central dans l'accompagnement des patients diabétiques de type 2 dans un trajet de soins ou un trajet de démarrage », explique le professeur De Block. « Dans ce cadre, il peut être utile de recourir à la surveillance continue de la glycémie. Et quand on sait ce qu'il faut surveiller, l'interprétation des données ne prend vraiment pas beaucoup de temps. »
Le professeur De Block propose cinq étapes à cet effet :
- Dispose-t-on de suffisamment de données ?
- Y a-t-il des périodes d’hypoglycémie (TBR), avec des valeurs ≤ 70 mg/dl, et si oui, s’agit-il d’hypoglycémie nocturne et/ou sévère (≤ 54 mg/dl) ? Quelle pourrait en être la cause (activité physique accrue, consommation réduite d’hydrates de carbone, … ?)
- Quel est le temps passé dans la fourchette cible (TIR) ?
- Quelle est la variabilité (CV) ? Y a-t-il de nombreuses fluctuations ? Sont-elles explicables ? Pensez à l'activité physique, aux fêtes, aux collations du soir…
- Y a-t-il une stabilité ? Comparez le profil actuel avec les périodes précédentes.
Sur la base de ce qui précède, un plan d'action peut être convenu avec le patient.
En pratique
Prof. De Block geeft twee voorbeelden uit de dagelijkse praktijk waar het gebruik van CGM een substantieel verschil uitmaakte.
Cas n° 1
Une femme de 70 ans, atteinte de DT2 depuis 2016, sans complications. Comorbidités : hypertension, hypercholestérolémie et antécédents d'AIT. Elle est traitée par 850 mg de metformine deux fois par jour, un inhibiteur du SGLT2 et de l'insuline basale.
Elle mesure quotidiennement sa glycémie à jeun et, en outre, deux fois par semaine, sa glycémie quatre fois par jour ; ses résultats sont bons et se situent toujours entre 60 et 140 mg/dl. Pourtant, son taux d'HbA1c est bien plus élevé que ce à quoi nous nous attendions. Le rapport LibreView indique ce qui suit :

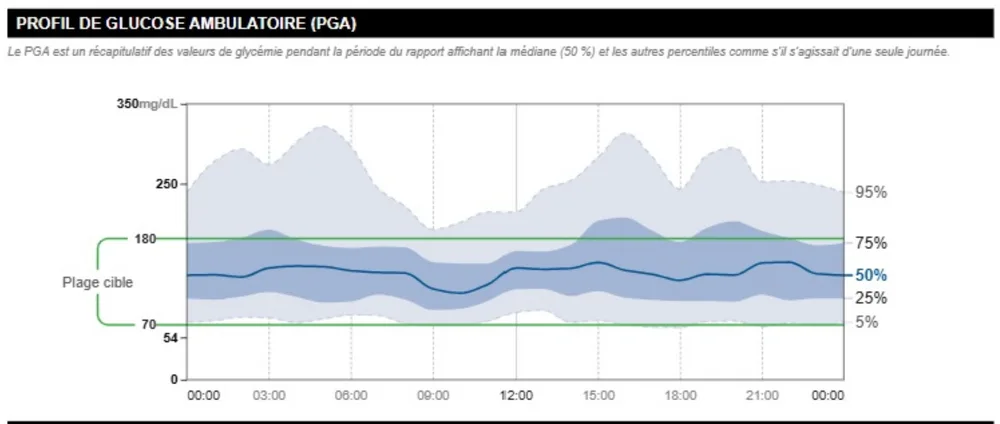
Le temps passé en hypoglycémie est élevé (7 %), le temps passé dans la fourchette cible n'est que de 54 %, et on observe en plus une très grande variabilité. On remarque qu'une très forte augmentation de la glycémie se produit au cours de la soirée (responsable de l'HbA1c plus élevée que prévu), suivie d'une forte baisse pendant la nuit et d'une glycémie qui se normalise vers le matin (mesurée comme une glycémie à jeun normale). Il ressort d’une anamnèse ciblée qu'elle grignote souvent (beaucoup et des aliments riches en sucre) au cours de la soirée en raison d'une énorme peur de l'hypoglycémie nocturne. On lui conseille d'arrêter cette pratique et, lors d'une consultation suivante, on observe une courbe plus régulière et une valeur d'HbA1c plus basse. La patiente continue d'utiliser un capteur afin d'être avertie par des alarmes si sa glycémie venait à baisser pendant la nuit.
La crainte de cette patiente de faire une hypoglycémie n'est pas tout à fait injustifiée : des études montrent que la fréquence de l'hypoglycémie nocturne chez les personnes atteintes de DT2 est souvent fortement sous-estimée.(7)
Cas n° 2
Un homme de 62 ans, atteint de DT2 depuis l'âge de 51 ans, traité par 850 mg de metformine deux fois par jour et par une sulfonylurée. Il présente une rétinopathie non proliférative légère et une polyneuropathie. Il boit deux verres de vin par jour et mange beaucoup de sucreries. Son HbA1c a fortement augmenté ces derniers temps et il demande maintenant de lui-même à utiliser un capteur. Il apparaît rapidement qu'il y a surtout de nombreux pics postprandiaux et que la valeur avant le coucher est également élevée. On lui demande de réduire sa consommation d'alcool, ainsi que les portions de glucides lors des repas et les grignotages, et de faire désormais aussi une longue promenade quotidienne. Résultat : son HbA1c passe de 8,2 à 6,7 % et il a perdu 3 kg. Il est maintenant très motivé pour poursuivre ce mode de vie.
HbA1c et Time in Range
L'HbA1c est le paramètre utilisé depuis des décennies pour suivre le contrôle glycémique, mais il s'agit en réalité plutôt d'un paramètre de substitution qui est également influencé par des facteurs tels que la durée de vie des globules rouges, ce qui n'a rien à voir avec l'exposition au glucose.(8)
« L'HbA1c est et reste certainement un paramètre précieux », déclare le professeur De Block, « mais il ne nous renseigne pas sur les fluctuations quotidiennes. C'est pourquoi les données issues des mesures continues de la glycémie, telles que le TIR et la variabilité, constituent le complément idéal. Ensemble, elles offrent une image plus complète et nous permettent de mieux voir où et comment intervenir. »
« Enfin, de plus en plus d'études démontrent le lien entre le TIR et les complications à long terme,(9) », conclut le professeur De Block, « et il ne fait aucun doute que de nombreuses autres recherches seront menées à ce sujet à l'avenir. »
Références
1. Wilmot, Emma G., Moore, Peter, et al. “Continuous glucose monitoring versus self-monitoring of blood glucose in individuals with type 2 diabetes: a randomised, multicentre, open-label, superiority trial.” The Lancet Diabetes & Endocrinology, 2026.
2.Aronson, Robert, Brown, Rebecca E., et al. “Impact of flash glucose monitoring in people with type 2 diabetes inadequately controlled with non-insulin antihyperglycaemic therapy (IMMEDIATE): A randomized controlled trial.” Diabetes, Obesity and Metabolism, vol. 25, no. 4, 2023, pp. 1024–1031.
https://doi.org/10.1111/dom.14944
3. Ajjan, Ramzi A., Battelino, Tadej, et al. “Continuous glucose monitoring for the routine care of type 2 diabetes mellitus.” Nature Reviews Endocrinology, vol. 20, no. 7, 2024, pp. 426–440. https://doi.org/10.1038/s41574-024-00978-7
4. Polonsky, William H., Soriano, Emilyn C., et al. “Does continuous glucose monitoring use prompt greater engagement in self-management? A randomized controlled trial focusing on adults with type 2 diabetes.” Journal of Diabetes Science and Technology, 2025, article 19322968251361031. https://doi.org/10.1177/19322968251361031
5. Alva, Steven, Bailey, Tim, et al. “Accuracy of a 14-day factory-calibrated continuous glucose monitoring system with advanced algorithm in pediatric and adult population with diabetes.” Journal of Diabetes Science and Technology, vol. 16, no. 1, 2022, pp. 70–77. https://doi.org/10.1177/19322968211019680
6.Battelino, Tadej, Danne, Thomas, et al. “Clinical targets for continuous glucose monitoring data interpretation: Recommendations from the international consensus on time in range.” Diabetes Care, vol. 42, no. 8, 2019, pp. 1593–1603. https://doi.org/10.2337/dci19-0028
7. Boureau, Anne-Sophie, Guyomarch, Benoît, et al. “Nocturnal hypoglycemia is underdiagnosed in older people with insulin-treated type 2 diabetes: The HYPOAGE observational study.” Journal of the American Geriatrics Society, vol. 71, no. 7, 2023, pp. 2107–2119. https://doi.org/10.1111/jgs.18392
8. Xu, Yanjun, Bergenstal, Richard M., Dunn, Timothy C., Ajjan, Ramzi A. “Addressing shortfalls of laboratory HbA1c using a model that incorporates red cell lifespan.” eLife, vol. 10, 2021. https://doi.org/10.7554/eLife.69420
9. De Meulemeester, Jonas, Charleer, Silke, et al. “The association of chronic complications with time in tight range and time in range in people with type 1 diabetes: A retrospective cross-sectional real-world study.” Diabetologia, vol. 67, no. 8, 2024, pp. 1527–1535. https://doi.org/10.1007/s00125-024-06143-6
© 2026 Abbott. Tous droits réservés. Libre et les marques associées sont des marques d'Abbott. ADC-2689426 v1.0
*La commercialisation du système FreeStyle Libre original a été interrompue sur les marchés de l'UE et du Royaume-Uni. Sur ces marchés, les systèmes FreeStyle Libre 2 et 3 sont disponibles ; ils offrent les mêmes avantages que le système FreeStyle Libre original, avec en plus la fonctionnalité optionnelle d'alarmes en temps réel.
L'utilisation et le remboursement en Belgique sont soumis aux critères fixés par l'INAMI (RIZIV).
Article rédigé en collaboration avec Abbott.
Le professeur De Block collabore avec Abbott, Minimed, Indigo Diabetes, Dexcom et Insulet, des entreprises qui développent des technologies pour le diabète.

